- Открытия
Рибофлавин на прицеле у онкологов
Как показали исследования группы ученых, комплекс из рибофлавина и наночастиц может стать инструментом целенаправленного воздействия на опухоль

Витамин В2, или рибофлавин, играет ключевую роль транспортера энергии в клетку. Это единственный витамин, не вызывающий гипервитаминоза: им невозможно отравиться, избыток легко выводится; его производные входят в состав многих важнейших ферментов, поэтому В2 – одно из главных для здоровья веществ.
В одном из интервью Евгений Хайдуков пошутил: «Чтобы нормально конкурировать с Западом (а все-таки научный мир – это конкурентный мир), мы стараемся браться за очень простые идеи, простые решения. Русская смекалка, преимущество русского мира. Если на Западе берут какого-то специалиста из другой страны, то они понимают, что учился он колеса крутить – все, он будет только колеса крутить. А если приезжает русский, все понимают, что он может и колеса крутить, и ядерную бомбу собрать».
Наночастица (nanoparticle) – изолированный твердофазный объект, имеющий отчетливо выраженную границу с окружающей средой, размеры которого во всех трех измерениях составляют от 1 до 100 нанометров (нанометр – одна миллиардная часть, 10-9 метра).
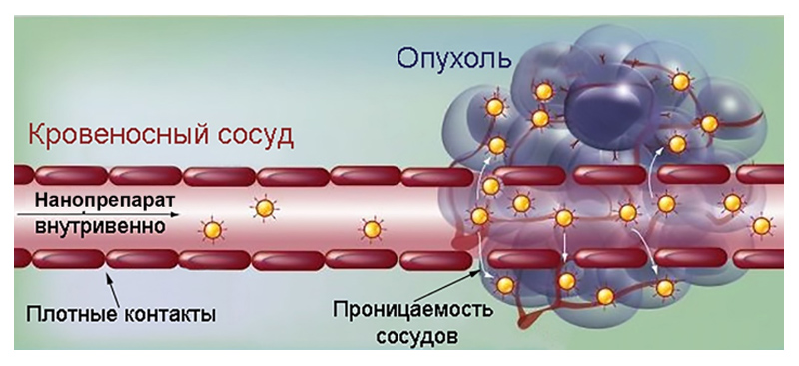
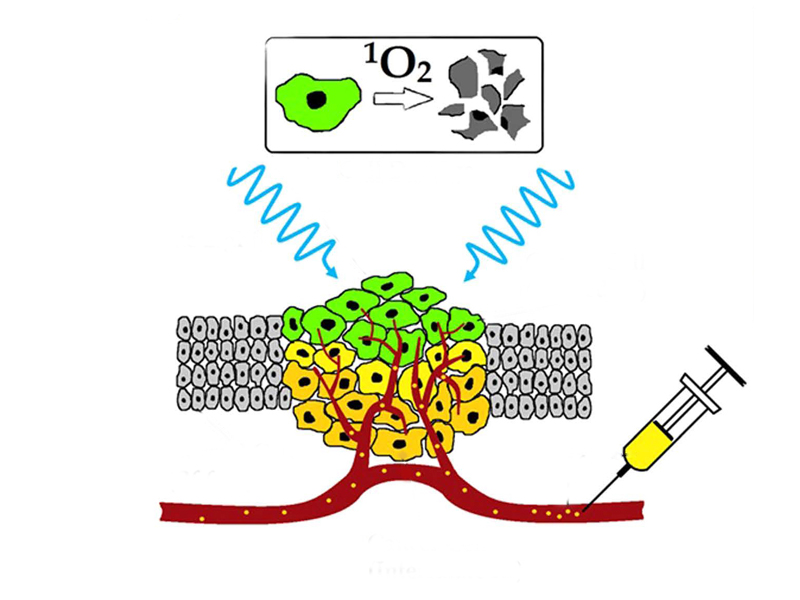
Принцип пассивной доставки
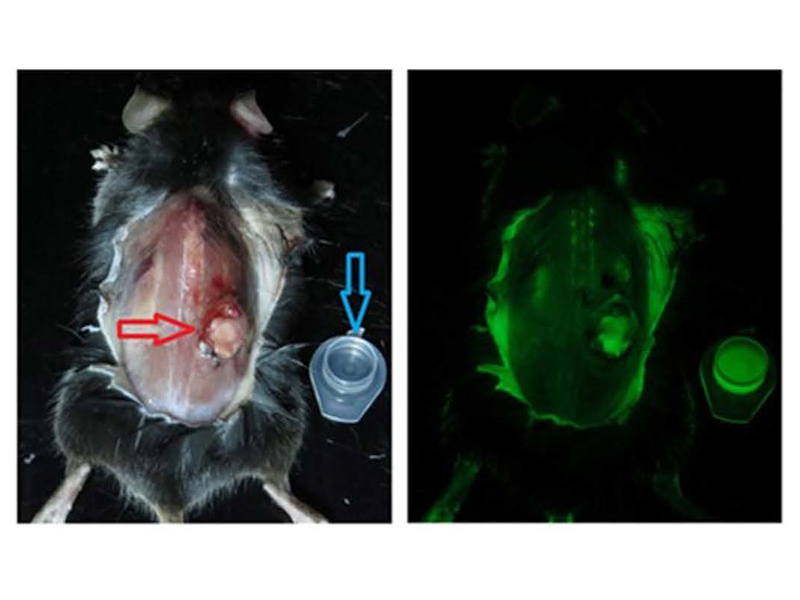
Внутривенное введение препарата рибофлавина и картина состояния опухоли у мыши. Источник — Scientific Reports
1/2
Внутривенное введение препарата рибофлавина и картина состояния опухоли у мыши. Источник — Scientific Reports
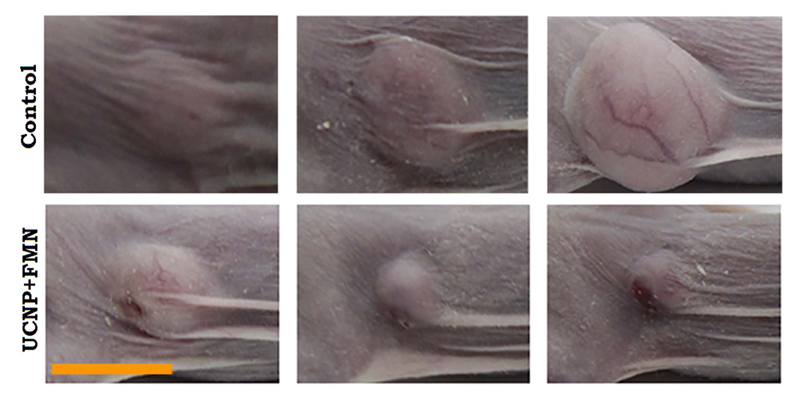
Наглядная демонстрация уменьшения опухоли у мыши. Источник — Scientific Reports
Рекомендованные материалы
Практики, Здоровье@mail.ru
5 супертехнологий лечения рака, доступных уже сегодня
В одной раковой опухоли может быть несколько разных мутаций — и для борьбы с каждой требуется свое оружие
Тема: Удивительное здравоохранение
Открытия
Сибирские ученые намерены дополнить иммунотерапию рака
Они разрабатывают новые лекарства
Тема: Удивительное здравоохранение
Развитие, РИА Новости
«Сколько больных – столько видов рака»
Как лечат самые агрессивные виды оноклогии
Тема: Удивительное здравоохранение